新闻动态
2020年12月3日,中国药品监督管理研究会、清华大学老科协医疗健康研究中心与社会科学文献出版社联合发布了《医疗器械蓝皮书:中国医疗器械行业发展报告(2020)》。
2019年,我国医疗器械行业在监管政策不断完善、市场竞争更加激烈、集中招标采购规模逐步扩大、国际市场复杂多变的情况下,继续保持了良好的发展势头,生产企业数量、主营业务收入、研发投入、进出口贸易等继续增长。全国药品监督管理部门深入推进医疗器械审评审批制度改革,持续加强医疗器械全生命周期严格监管,不断强化法规标准基础建设,各项工作取得新成效,有力地推动了我国医疗器械行业的健康快速发展。
本书从多角度论述了2019年影响医疗器械行业发展的政策变化态势。审批制度改革方面,提出要不断健全医疗器械标准管理体系、加强医疗器械分类管理与医疗器械检验检查能力等;医疗器械上市后监管方面,建议加快推进法规制度建设、全面推进风险会商、加强疫情防控医疗器械质量监管等;对2019年不良事件监测数据进行了分析与解释,并提出应通过对不良事件报告的积极收集、分析,有针对性地采取风险控制措施,降低产品风险;为更好地应对突发公共卫生事件,对我国医疗器械应急审批程序和相关法律要求进行了总结;审评制度改革方面,建议积极推进智慧审评、提高审评科研水平、有效运行审评科学管理体系等;在总结2019年典型省(区、市)、地市耗材集中采购特点的基础上,提出2020年国家集中采购将常态化,各省(区、市)将会利用省级集中采购平台广泛地进行带量采购;2019年医疗器械注册人制度试点范围进一步扩大,产业创新活力得到激发。
最后,在新冠肺炎疫情暴发背景下,本书对我国医疗器械供给保障制度和机制、应急医用物资保障体系进行了探讨,对即时检测(POCT)技术应用、医疗器械产品上市审批、ECMO应用等进展进行了思考。
《医疗器械蓝皮书:中国医疗器械行业发展报告(2020)》
我国医疗器械对外贸易结构继续优化,高端医疗器械核心部件研发力度仍需加大
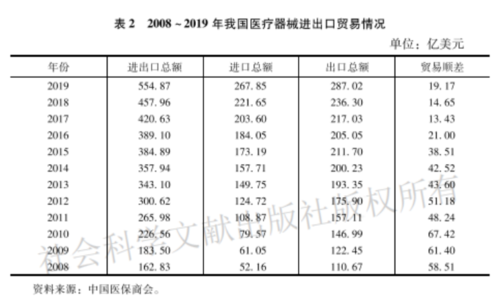
蓝皮书指出,据中国医保商会统计资料,我国医疗器械进出口贸易保持11年持续增长势头(见表2)。2019年我国医疗器械进出口总额为554.87亿美元,较上年增长21.16%。其中,进口额267.85亿美元,同比增长20.84%;出口额287.02亿美元,同比增长21.46%。总体上看,我国医疗器械对外贸易结构继续优化,高端医疗器械产品所占比重有所增加,质量效益持续改善,比较好地适应了国际市场的需求和复杂变化,经受住了不断加剧的贸易摩擦考验。在我国对外贸易总体环境复杂多变的大形势下,我国医疗器械产品对外贸易取得这样的成绩实属不易。这得益于国家有关政策的支持,更得益于医疗器械行业的不断创新、众多医疗器械企业的开拓进取。
蓝皮书指出,在高端医疗器械领域,国外产品如高端X光CT、磁共振诊断仪、纤维内窥镜、手术机器人、体外膜肺氧合(ECMO)等还占据我国三级医院的主要市场,有些高端医疗器械的核心部件国内还不能生产,需要依赖进口。我国的医疗器械研发、生产企业需要在这些方面加大创新研发力度,尽快赶超国际先进水平。
未来一年我国医疗器械行业仍将处于“黄金发展期”
1. 政治环境有利于我国医疗器械行业健康发展
在习近平新时代中国特色社会主义思想指引下,党中央、国务院高度重视医疗器械产业发展,不断深化有关改革措施,先后出台有关政策,鼓励支持高端医疗器械发展。当前我国社会政治稳定,经济发展,人民群众生活水平持续提高,全面建成小康社会目标将如期实现,医疗保障水平也将逐年提高。2020年初以来,为了防控新冠肺炎疫情,国家出台了新一轮减税降费等促进企业发展的政策。这些都为我国医疗器械行业健康快速发展提供了良好的社会政治环境。
2. 经济环境有利于我国医疗器械行业健康发展
2019年,我国经济继续健康发展,国民经济增速保持在6%左右。许多地方政府出台优惠政策支持医疗器械产业发展,有的地方不仅给予医疗器械生产企业税费减免优惠政策,还给予医疗器械产品注册奖励、产品创新奖励、生产厂房房租补助等。从整个经济环境来看,这些优惠政策有利于我国医疗器械行业的健康发展。
3. 国家扶贫政策和医疗保障政策调整有利于医疗器械产业发展
为了实现2020年脱贫攻坚的宏伟目标,在党中央、国务院扶贫政策推动下,许多地方政府出台特殊补助政策,如大病医疗费二次报销、提高贫困人口医疗费用报销比例等。全国医疗卫生机构门诊人次、住院人次持续增加,推动了全社会医疗器械需求不断增长。
4. 随着国家多项鼓励科技创新政策的实施,医疗器械创新发展呈现加速之势
随着国家各项鼓励科技创新政策的实施,医疗器械研发机构,特别是医疗器械生产企业创新研发内在动力将大增,全社会医疗器械总的研发投入将连年大幅增长,创新医疗器械申报数量将连年增加,创新医疗器械产品将加速涌现。
5. 国内外医疗器械市场的不确定因素增多
首先,国家实行医疗器械集中带量招标采购、重点产品监控、取消加成、鼓励实行“两票制”、医用耗材医保准入机制等政策必然会影响医疗器械市场价格,这对医疗器械销售规模的影响存在着不确定性;其次,国际贸易保护主义抬头,特别是中美贸易摩擦必将影响我国医疗器械出口增速;再次,为了适应带量招标采购的价格竞争,可能有的医疗器械生产企业为了降低产品成本会降低产品质量,这有可能增加医疗器械不合格风险。
综合分析我国医疗器械行业面临的形势,蓝皮书课题组认为:我国医疗器械行业虽然面临诸多方面的挑战,但是依然表现出旺盛发展活力,发展前景广阔;国家医疗器械监管法规政策将继续完善,审评审批制度改革将继续深化,上市后监管力度将进一步加大;创新医疗器械将加速涌现,将有更多创新医疗器械特别是防治新冠肺炎的医疗器械获准注册上市;我国医疗器械行业将继续保持健康发展的良好势头,但增长幅度可能会减小;医疗器械进出口贸易总额将继续增长,但增长幅度很可能会有所下降。总之,未来一年我国医疗器械行业仍将处于“黄金发展期”。
医疗器械不良事件监测为我国医疗器械监管事业发展提供有力支撑
蓝皮书指出,医疗器械不良事件监测是强化医疗器械全生命周期监管、严防严控医疗器械上市后风险的重要举措,也是医疗器械监管的重要环节。对于医疗器械生产企业,不良事件监测既是法规要求,也是质量管理体系的重要组成部分,更是一个企业能够健康生存发展的内在需要。医疗器械被批准上市,说明经过设计、开发、确认、验证、动物实验、临床试验/评价等过程,以及技术审评,和已知收益相比产品的已知风险较低,产品是一个风险可接受产品。但由于产品上市前的研究和临床试验/评价的局限性,这只是一个阶段性结果判断。产品上市后大规模使用的实际风险情况往往与上市前研究的结果有一定差别,部分产品除了表现出已知风险之外,还可能出现非预期风险或者出现已知风险的非预期增大情况,只有对上市后的医疗器械开展广泛的、全面的监测才能够有效地发现、识别、控制这些额外的风险,保障医疗器械使用者、患者的健康和安全。
2019年新版《医疗器械不良事件监测和再评价管理办法》是由国家市场监督管理总局、国家卫生健康委员会联合发布的,其对医疗器械不良事件的定义为“已上市的医疗器械,在正常使用情况下发生的,导致或者可能导致人体伤害的各种有害事件”。对严重伤害情形的定义,2019年新版《医疗器械不良事件监测和再评价管理办法》与2008版相比未做改动。对比两版《医疗器械不良事件监测和再评价管理办法》,可以看出2019年新版《医疗器械不良事件监测和再评价管理办法》删除了关于质量合格的要求,大大扩展了医疗器械不良事件的内涵,将2008版《医疗器械不良事件监测和再评价管理办法》中的医疗器械质量事故也包含于不良事件监测工作中。
医疗器械不良事件内涵的扩大反映了医疗器械不良事件监测工作在监管工作中的地位不断提高,作用越来越显著,对风险的发现和控制能力越来越强,也与国际上医疗器械不良事件监测工作由监测向警戒发展的趋势相一致。2019年8月26日第十三届全国人民代表大会常务委员会第十二次会议审议通过的《中华人民共和国药品管理法(2019修订版)》第十二条规定“国家建立药物警诫制度,对药品不良反应及其他与用药有关的有害反应进行监测、识别、评估和控制”,从既往的药品不良反应报告制度到药物警诫制度,这一转变具有里程碑意义,是我国药品监督管理制度的重大进步。医疗器械不良事件监测内涵的扩展正是监管在这一背景下的新探索、新发展,必将为我国医疗器械监管事业的跨越式发展提供强有力的支撑。
相关阅读推荐
报告精读 | 医疗器械蓝皮书:中国医疗器械行业发展报告(2019)
报告精读 | 医疗器械蓝皮书:2018年医疗器械行业十大发展趋势全景展望
报告精读 | 中国医疗器械行业发展报告(2017)
精彩目录
Ⅰ总报告
1. 2019年我国医疗器械行业形势分析及2020年展望
一、 2019年我国医疗器械行业形势分析
二、 2019年我国医疗器械行业监管情况
三、 2019年我国医疗器械监管体制改革和法规建设情况
四、 未来我国医疗器械行业发展面临的环境及前景展望
Ⅱ政策篇
2. 2019年我国医疗器械审批制度改革分析报告
3. 2019年我国医疗器械上市后监管改革报告
4. 2019年我国医疗器械不良事件监测报告
5. 2019年我国医疗器械应急审批报告
6. 2019年医疗器械审评制度改革报告
7. 2019年我国医用耗材集中采购状况及展望
8. 2019年我国医疗器械行业政策分析报告
9. 2019年我国医疗器械注册人制度试点实施报告
Ⅲ行业篇
10. 2019年我国医疗器械对外贸易状况和发展趋势
11. 2019年我国医疗器械标记合规性问题分析报告
12. 2019年我国医疗器械检验检测能力分析与展望
13. 2019年我国医疗器械临床试验质量问题分析
14. 2019年我国医疗机器人行业发展报告
15. 2019年我国伴随诊断产业发展状况及趋势分析
16. 2019年我国骨科植入物行业状况和发展趋势分析
Ⅳ市场篇
17. 2019年我国医用防护性物资使用情况与发展趋势分析
18. 2019年我国外科吻合器行业发展状况和发展趋势
19. 2019年我国数字化技术在口腔医疗器械领域应用分析报告
20. 2019年我国左心耳封堵器市场状况及发展趋势
21. 2019年我国颅内脑电采集器械行业发展状况与趋势分析
22. 2019年我国眼前段植入式器械的应用状况与展望
Ⅴ区域篇
23. 2019年北京市医疗器械行业发展状况与展望
24. 2019年上海市医疗器械行业发展状况与展望
25. 2019年广东省医疗器械行业发展状况与展望
26. 2019年江苏省医疗器械行业发展状况及展望
27. 2019年湖北省医疗器械行业发展状况与展望
28. 2019年云南省医疗器械行业发展状况与展望
29. 2019年内蒙古自治区医疗器械行业发展状况与展望
Ⅵ实践篇
30. 对深圳市医疗器械产业韧性的思考
31. 邯郸市医保耗材带量采购模式探讨
32. 对医疗器械注册人制度下责任风险及认知误区的思考
33. 我国碳离子治疗系统的研发和上市应用
34. 我国医疗器械产业园现状与综合实力评估
35. 多模式一体化放疗设备的发展现状与展望
36. 医疗器械CDMO新业态下第三方机构的参与机制分析
Ⅶ热点篇
37. 对突发事件下我国医疗器械供给保障制度和机制的探讨
38. 对我国应急医用物资保障体系建设的思考与建议
39. 即时检测在应对突发传染病疫情中的实践和思考
40. 新冠肺炎疫情下我国医疗器械产品上市审批情况分析
41. 我国新冠肺炎防治中ECMO的应用进展
42. 后记
43. 《中国医疗器械行业发展报告(2021)》征稿函
如需《医疗器械蓝皮书:中国医疗器械行业发展报告(2020)》电子书请前往皮书数据库进行购买






 京公网安备 11010202008210号
京公网安备 11010202008210号
0 人参与 0 条评论(查看)
网友评论